Die IEC 62443-4-1 ist Teil einer Normenfamilie zur „IT-Sicherheit für industrielle Automatisierungssysteme“.
Dieser Artikel stellt Ihnen den Teil 4-1 vor, der Anforderungen an den Lebenszyklus (Entwicklung, Wartung) von sicheren Produkten stellt. Er untersucht auch, ob diese Norm für Hersteller von Medizinprodukten sinnvoll anwendbar ist.
1. Die Normenfamilie IEC 62443
a) Übersicht
Die IEC 62443 ist eine ganze Familie an Normen zur IT-Sicherheit von industriellen Automatisierungssystemen:
- Anforderungen an den Lebenszyklus für eine sichere Produktentwicklung: DIN EN IEC 62443-4-1
- Sicherheitsrisikobeurteilung und Systemgestaltung: DIN EN 62443-3-2
- Anforderungen an Komponenten industrieller Automatisierungssysteme: DIN EN 62443-4-2
- Anforderungen an das IT-Sicherheitsprogramm von Dienstleistern für industrielle Automatisierungssysteme: DIN IEC 62443-2-4
- Systemanforderungen zur IT-Sicherheit und Security-Level: DIN IEC 62443-3-3
Ein Teil dieser Normen befindet sich noch in der Entwicklung.

Dabei wendet sich die Serie 4 v.a. an die Entwickler bzw. Lieferanten, die Serie 3 an die Integratoren und die Serie 2 an die Betreiber.
b) Anwendungsbereich
Bereits der Titel der Normenfamilie macht deren Anwendungsbereich klar: Industrielle Automatisierungs- und Steuerungssysteme. Allerdings enthält die Norm nur Anforderungen, die für andere Produktklassen als ebenso sinnvoll erscheinen.
2. IEC 62443-4-1
a) Anwendungsbereich
Der Teil 4-1 möchte Anforderungen an den kompletten Lebenszyklus stellen einschließlich Entwicklung und Wartung. Diese Anforderungen betreffen:
- Anforderungsspezifikation
- Entwurf, Architektur
- Implementierung einschließlich Kodierrichtlinien
- Verifizierung
- Validierung
- Management von Fehlern und Patches
- Außerbetriebnahme
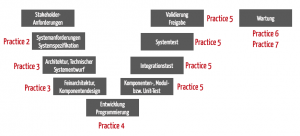
Hingegen fühlt sich die IEC 62443-4-1 nicht für die Integration und die Anwendung des Produkts zuständig. Diese finden sich in den Serien 2 und 3 dieser Normenfamilie.
b) Aufbau
Die Norm besteht im Wesentlichen aus acht „Ansätzen“ (wie das die Deutsche Norm den Begriff „Practices“ übersetzt).
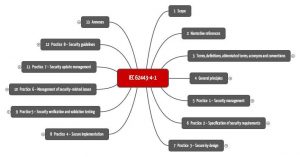
Jeder dieser Ansätze umfasst zwischen zwei und 13 Aspekten. Für jeden Aspekt formuliert die IEC 62443-4-1 jeweils ein oder mehrere Anforderungen und gibt eine Begründung dafür.
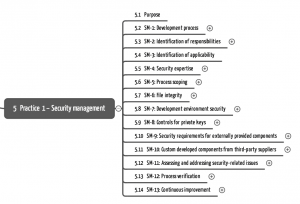
Hier PDF mit Mindmap (ausgeklappt) zum Download
c) Anforderungen
Die acht „Ansätze“ (Themengebiete) adressieren den Lebenszyklus von IT-Systemen einschließlich der Wartung und der Dokumentation, die bei Medizinprodukten dem „Labeling“ entspricht.
| „Ansatz“ | Beispiele für Anforderungen |
| 1. Verwaltung der IT Sicherheit |
|
| 2. Spezifikation der IT-Sicherheitsanforderungen |
|
| 3. IT-Sicherheit durch Entwurf |
|
| 4. Gesicherte Implementierung |
|
| 5. Verifikatons- und Validierungsprüfungen der IT-Sicherheit |
|
| 6. Behandlung sicherheitsbezogener Probleme |
|
| 7. Verwaltung von IT-Sicherheits-Updates |
|
| 8. IT-Sicherheitsrichtlinien |
|
Vergleich und Zusammenspiel mit anderen Normen
Die IEC 62443-4-1 basiert auf weiteren Normen und Dokumenten wie der IEC 15408-3, der IEC 61508 und dem RTCA DO-178B. Sie verweist zudem auf den „The Security Development Life-cycle” von Michael Howard und Steve Lipner, den auch Microsoft nutzt bzw. referenziert.
Die Normen der Familie UL 2900 finden keine Erwähnung, obwohl der Scope teilweise vergleichbar ist.
Bewertung, Fazit
a) Eine verständliche und systematische Norm
Die IEC 62443-4-1 ist (im Gegensatz zum UL 2900) eine klar formulierte und strukturierte Norm. Sie macht deutlich, dass IT-Sicherheit nur erreicht werden kann (falls überhaupt), wenn sie über den kompletten Lebenszyklus eines Produkts beachtet wird.
Die Anforderungen sind in gewisser Weise „common sense“. Die Verwundbarkeit der meisten Produkte und Systeme liegt aber darin begründet, dass die Hersteller genau diese Anforderungen nicht berücksichtigen. Diese Anforderungen zusammengetragen zu haben, macht den Wert dieser Norm aus.
Die Übersetzung ins Deutsche ist hingegen etwas holperig geraten.
b) Etwas high-level
Die Anforderungen der Norm sind etwas „high level“. Sie gibt beispielsweise nicht vor, über welche Kompetenzen die Verantwortlichen verfügen müssen, sie erklärt nicht, was getan werden muss, um das Produkt während seiner Entwicklung zu schützen. Die Norm spricht von Kodierrichtlinien, ohne konkrete Beispiele dafür zu formulieren.
Konkrete Hinweise zur Umsetzung finden sich (leider nur und auch dort nur teilweise) bei den Begründungen und weiteren Hinweisen. Damit eignet sich die Norm eher für Prozessmanager als für Entwickler.
Das ist jedoch keine Kritik. Denn die Norm formuliert zumindest die Aspekte, welche die Hersteller bei der Entwicklung und Wartung von Produkten bezüglich der IT Security beachten müssen.
c) Hilfreich aber nicht ausreichend für Medizinproduktehersteller
Die IEC 62443-4-1 sieht ihren Anwendungsbereich zwar bei industriellen Automatisierungssystemen. Allerdings enthält die Norm keine Anforderungen, die sich nicht unverändert auf die Entwicklung und Wartung vernetzter Medizinprodukte übertragen lassen.
Umgekehrt berücksichtigt der Leitfaden keine Anforderungen, die spezifisch für Medizinprodukte sind wie die Safety und das (medizinische) Risikomanagement. Weil der Norm der Branchenfokus fehlt, könnte man die darin formulierten Anforderungen als notwendig aber als nicht als hinreichend bezeichnen.
Die FDA zählt andere und veraltete Mitglieder der Normenfamilie zu den recognized standards, nicht aber die IEC 62443-4-1.
d) Kleinere Logikbrüche
Die Zuordnung der Aktivitäten zu den Lebenszyklus-Phasen ist nicht in allen Fällen nachvollziehbar. Wie sollen vor(!) dem Entwurf bereits interne Protokolle bekannt sein, die die Norm bereits beim Threat Modelling während der Anforderungsphase analysiert haben will?
Umgekehrt verlangt die Norm die Spezifikation der externen Schnittstellen erst beim Entwurf.
Die Metriken im Anhang sind teilweise sehr „C-lastig“ und können eine nicht ganz berechtigte Illusion einer Genauigkeit erwecken.
e) Grundlage für eine Zertifizierung?
Viele Prüfhäuser und benannte Stellen bieten Zertifizierungen nach IEC 62443 an. Überdenken Sie immer den Wert von Zertifikaten, insbesondere in den folgenden Fällen:
- Ein Zertifikat wird nicht unter dem Dach der DaKKS ausgestellt. Solch ein Zertifikat kann jeder erstellen.
- Die Prüfung erfolgt nicht gemäß einer Prüfnorm.
- Die Norm, deren Konformität geprüft werden soll, enthält weder testbare Anforderungen noch Hinweise zu deren Prüfung.
- Die Norm, deren Konformität geprüft werden soll, ist keine harmonisierte Norm.
Damit sei nicht von diesen Zertifizierungen abgeraten. Vielmehr sollen die Hoffnungen auf einen „sicheren“ Konformitätsbeweis relativiert werden.
f) Hoher Preis und eine Alternative
Mit 270 CHF ist die Norm vergleichsweise teuer. Trotzdem sei sie zum Kauf empfohlen.
Der Leitfaden zur IT Sicherheit für Medizinprodukte, den das Johner Institut gemeinsam mit dem TÜV Süd entwickelt hat, enthält vergleichbare Anforderungen, ist noch spezifischer für Medizinprodukte und dabei kostenlos. Er ist ab dem 22.11.2018 verfügbar.





im Navigator zuoberst rechts hat es einen kleinen Druckfehler:
IST 62443-5-1
SOLL 62443-4-1
Vielen Dank für das Lesen, Zusammenfassen und Aufbereiten.
Peter Pianegonda
Sie haben ja so Recht! Danke, lieber Herr Pianegonda!
Danke Ihrer Hilfe konnte ich den Fehler korrigieren. Danke!
Hallo,
wo ist denn der Leitfaden von Ihnen und dem TÜV Süd verfügbar?
Sie können den Leitfaden hier herunterladen
Hallo Herr Johner,
sie schreiben in ihrem Leitfaden: „Es besteht in Europa (im Gegensatz zu den USA) auch keine Pflicht, ein spezifisches Dokument zur IT-Sicherheit
zu erstellen.“
Frage dazu: Ist mit dem spezifischen Dokument hier die „Cybersecurity Bill of Materials (CBOM)“ gemeint?
Viele Grüüße, C. Beck
Hallo Christian,
mal wieder eine super Analyse und Darstellung eines Standards 🙂
Mir fällt dabei auf, dass keine der 57 Aspects oder 8 Practises „Security Risk“ explizit benennt.
Risk Management ist ja ein zentraler Aspekt bei Medical Devices (MD), insbesondere vernetzte MDs (ISO/IEC 80001 family).
Die AAMI TIR57 stellt den Zusammenhang zwischen Security & Safety Risks gut dar, orientiert sich dabei aber leider an NIST 800, die eher ganze Organisationen betrifft.
Vielleicht sollte man als Fazit darauf hinweisen, dass es eine spezifische IEC 62443-3-2 „security risk assessment process“ als der der Standards-Family gibt. Dies sollte meiner Ansicht nach ein zentraler Teil eines Secure product development lifecycle sein.
Note: „security risk assessment“ ist sehr spezifisch, braucht damit spezielle Guidelines (s.a. AAMI TIR57), und es reicht nicht, dies mit einem Satz a là „risk management requirements are woven into the requirements throughout the product life cycle“ abzuhandeln.
Beste Grüße
Gilbert
Lieber Gilbert, ich stimme Dir absolut zu! Das werde ich aktualisieren!
Im IT-Security-Leitfaden haben wir die Aktivitäten explizit in den Software-/Produktlebenszyklus mit eingewoben. Dieser Leitfaden wird inzwischen auch bei Behörden und benannten Stellen als Standard referenziert, genannt und genutzt.
Liebe Grüße, Christian
Naja, also ob die 62443 so empfehlenswert ist, da bin ich mir nicht sicher. Wir fertigen beispielsweise Produkte für Industriekomponenten und überlegen, nach -4-2 zertifizieren zu lassen. In der -4-2 steht drin, als common requirement, dass die Komponente nach -4-1 entwickelt worden sein muss. Eine explizite Anforderung, ob jetzt eine -4-1 Zertifizierung erforderlich ist, steht allerdings nicht drin. Und obwohl wir bei uns natürlich nach modernem SDLC entwickelt und so wohl auch die Anforderung nach -4-1 bestehen würden, kriege ich von KEINEM der üblichen Verdächtigen Zertifizierer eine klare Antwort auf die popeleinfache Frage:
Brauche ich eine -4-1 Zertifizierung als Vorbedingung für eine -4-2 Zertifizierung?
Neee. Nur rumgewiesel „lassen Sie uns telefonieren“ blabla „kommt drauf an“. Auf eine JA oder NEIN Frage. Unfassbar, dass so eine simple Fragestellung mit HORRENDEN Auswirkungen auf die Zertifizierungskosten von der 62443 nicht KLIPP UND KLAR geregelt ist. Das ärgert mich.
Sehr geehrter Herr Schirmer,
danke für Ihre Gedanken.
Es geht in diesem Beitrag nicht um eine Zertifizierung. Eine Zertifizierung unter dem Dach der DaKKS gibt es für Medizinprodukte auch gar nicht. Damit sind alle entsprechenden Zertifikate nur bedingt wertvoll und erzwingen v.a. keine Konformitätsvermutung.
In anderen Beiträgen u.a. zur „Zertifizierung nach IEC 62304“ warnen wir sogar vor Beutelschneiderei durch Zertifzierungen.
Beste Grüße, Christian Johner