ISO 14969? Nie gehört? Sollten Sie aber. Denn an dieser Norm orientieren sich Ihre Auditoren beim ISO 13485-Audit.
Beachten Sie, dass die ISO 14969 eine Norm ist, die sich auf die ISO 13485:2003 bezieht. Für die ISO 13485:2016 nutzen Sie bitte den Practical Guide der ISO.
ISO 14969: Um was geht
Die ISO 14969 nennt sich Medizinprodukte Qualitätsmanagementsysteme – Anleitung zur Anwendung von ISO 13485. Und das sagt alles: Die ISO 14969 ist ein sogenannter „Technical Report, der erklärt, wie man die ISO 13485 verstehen und umsetzen kann.
Bei den Audits greifen Auditoren eher auf die ISO 14969 als auf die ISO 13485 zurück, wenn es mit dem auditierten Unternehmen Meinungsverschiedenheiten darüber gibt, wie man die ISO 13485 interpretieren oder umsetzen soll.
Aufbau des Technical Reports
Die ISO 14969 ist auf den oberen Ebenen genauso aufgebaut wie die ISO 13485; die Kapitelstruktur ist also identisch. Der Technical Report enthält sogar die ISO 13485: Jedes (Teil-) Kapitel beginnt mit dem normativen Text gefolgt von Erklärungen und Beispielen.
Allerdings ergänzt die ISO 14969 die ISO 13485 um eine weitere Kapitelebene, wobei diese Kapitel keine Überschriften tragen.
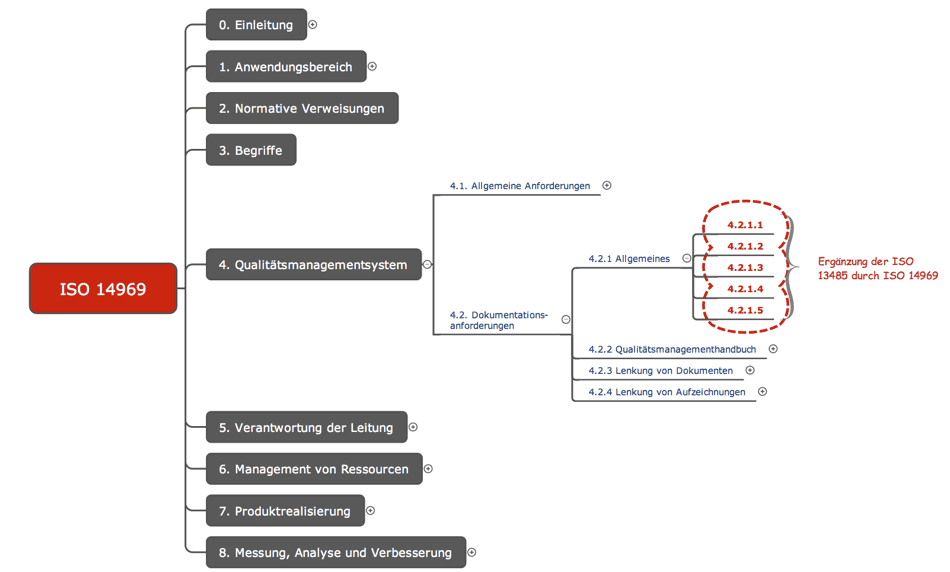
Abbildung 1: In rot markiert sind die Unterkapitel, um die die ISO 14969 die ISO 13485 ergänzt.
Beispiel
Die ISO 13485 fordert in 4.2.1 Folgendes:
Die Organisation muss eine Akte erarbeiten und aufrechterhalten, die für jeden Typ bzw. jedes Modell eines Medizinprodukts Dokumente entweder enthält oder auf den Standort dieser Angaben verweist, die Produktspezifikationen und Anforderungen an das Qualitätsmanagementsystem festlegen (siehe 4.2.3).
Die ISO 14969 schreibt genau dazu:
Die Akte für jeden Typ bzw. jedes Modell eines Medizinprodukts, auf die in ISO 13485:2003, 4.2.1, verwiesen wird, wird manchmal mit unterschiedlichen Begriffen bezeichnet. Diese Akte kann eine für die Herstellung dieses Produkts wesentliche Dokumentation enthalten oder auf deren Standort verweisen. Zu Beispielen solcher Dokumente gehören:
- Spezifikationen für Rohmaterialien, Kennzeichnung, Verpackungsmaterialien, Baugruppen und Medizinprodukte,
- Aufstellungen von Teilen,
- technische Zeichnungen,
- Softwareprogramme einschließlich des Quellencodes (falls verfügbar),
- Arbeitsanweisungen einschließlich des Betriebs der Ausrüstung,
- gegebenenfalls Einzelheiten über das Sterilisationsverfahren,
- Qualitätssicherungspläne,
- Verfahren der Herstellung und Prüfung, und
- Akzeptanzkriterien (Annahmekriterien).
Wie Sie sehen, konkretisiert und erläutert der Technical Report die ISO 13485.
Vorteile und Nachteile
Wenn Sie die ISO 14969 berücksichtigen, profitieren Sie von folgenden Vorteilen:
- Sie wissen, wie Ihre Auditoren denken und können sich besser auf Ihr Audit vorbereiten.
- Sie erhalten Unterstützung in Form von Beispielen und Erläuterungen beim Aufbau Ihres QM-Systems.
- Die klare Zuordnung von Forderungen der ISO 13485 zu den Erläuterungen vereinfacht das Lesen.
Allerdings sollten Sie auch Folgendes bedenken:
- Für die aktuelle ISO 13485:2016 gibt es den Technical Report nicht, allerdings den oben erwähnten Practical Guide. D.h. sie müssen nochmals Geld ausgeben.
- Das Dokument ist mit 97 Seiten deutlich umfangreicher als die „nackte“ QM-Norm. Sie müssen das auch lesen.
- Die ISO 14969 ist ein Technical Report – keine harmonisierte Norm.




Wird überhaupt an einer Revision der 14969 gearbeitet?
Ich habe auch etwas von einem handbook für die 13485 gehört, die anstatt der TR erscheinen soll, ist das korrekt?
danke
Ob an der Revision der 14969 gearbeitet wird, weiß ich nicht, ich gehe aber davon aus, dass dies folgen wird, da diese die Grundlage für die Arbeit der Auditoren ist.
Handbücher und Erläuterungen erscheinen ebenfalls, eines ist das von Randolph Ständer im Beuth-Verlag.
Sehr geehrter Professor Johner,
in der Berichtigung (aus Juli 2017, also nach dem Erscheinen dieses Blogthemas) zur DIN EN ISO 13485:2016 steht:
‚Im Europäischen Vorwort ist der vierte Absatz durch folgenden Absatz zu ersetzen:
„Dieses Dokument ersetzt EN ISO 13485:2012 und CEN ISO/TR 14969:2005.“ ‚
Darus folgt nach meinem Verständnis:
da es derzeit keinen Nachfolger der europäischen Version aus 2005 gibt, gilt sie durch die EN ISO 13485:2016
als ersetzt, also nicht mehr anwendbar.
Liege ich da richtig?
Viele Grüße
Boetcher
Sehr geehrter Herr Boettcher,
Sie haben Recht! Ich werde den Beitrag aktualisieren. Die ISO 14969 ist auch zurückgezogen.
Danke für Ihren wichtigen Hinweis, der mir hilft, diese Aktualisierung gleich nächstes Wochenende zu machen.
Beste Grüße, Christian Johner