Die ISO 19011 kennen leider nur wenige Medizinproduktehersteller. Dabei gibt ihnen diese Norm konkrete Hinweise, wie man Audits systematisch plant, durchführt, dokumentiert und nachbereitet.
Anwendungsbereich der ISO 19011
Diese Norm sollten Sie anwenden bei
- internen Audits nach ISO 9001 oder anderen Managementsystemen,
- internen Audits nach ISO 13485 und
- Audits bei Ihren Lieferanten.
Die benannten Stellen auditieren Ihr QM-System jedoch nach einer anderen Norm, der ISO 17021.
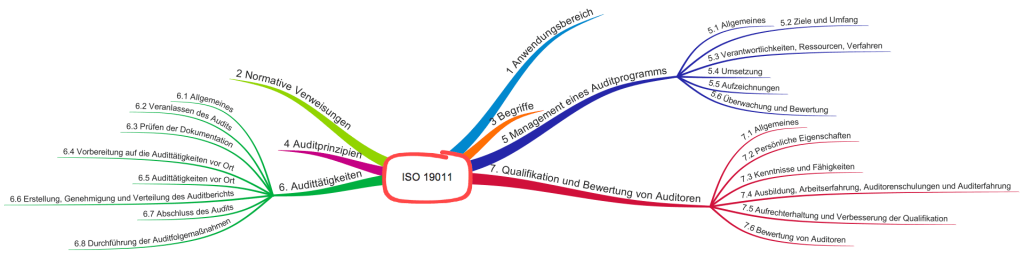
Inhalte der Norm
Die ISO 19011 enthält Folgendes:
- Begriffsdefinitionen wie Auditprogramm, Audit, Auditplan, Auditnachweise, Auditfeststellung und Auditkriterien. Nehmen Sie das nicht auf die ganz leichte Schulter: Ich war als Auditor dabei, wie eine Firma Audit, Auditprogramm und Auditplanung verwechselte. So etwas führt schnell zu einer „Non-Conformity“.
- Auditprinzipien: Hier geht es um die Prinzipien
- Ethisches Verhalten
- Sachliche Darstellung
- Berufliche Sorgfalt
- Unabhängigkeit
- Auf Nachweisen beruhende Vorgehensweise
- Audittätigkeiten
- Auditprogramm
- Audit: Planung, Durchführung, Berichtserstellung
- Qualifikation von Auditoren: Auch das kann bei Ihnen ein Thema sein. Die ISO 13485 verpflichtet Sie dazu, qualifiziertes Personal sicherzustellen. Gemäß ISO 19011 umfasst die Qualifikation Aspekte wie
- Persönliche Eigenschaften
- Kenntnisse und Fähigkeiten
- Ausbildung, (Auditoren-)Erfahrung, (Auditoren-)Schulung
Im Rahmen meiner eigenen Auditorenausbildung wurden wir in Fallstudien nach den Kriterien dieser Norm bewertet: Es gab Punkte für die richtige Begrüßung (ja, die ISO 19011 regelt sogar das), die passende Vorbereitung, das Stellen geeigneter Fragen, eine gute Zusammenfassung und Bewertung.
Was Sie tun sollten
Ihre internen Audits und Ihre Audits bei Ihren Lieferanten sind sehr wichtige Regelkreise Ihres QM-Systems.
- Die Norm beachten
Daher sollten Sie kompetente Personen beauftragen, diese Audits systematisch (nach allen Regeln der Kunst) durchzuführen. Verschwenden Sie keine Zeit darauf, sich zu überlegen, was unter „alle Regeln der Kunst“ zu verstehen ist. Die ISO 19011 sagt es Ihnen. Und wenn Sie über deren Forderungen hinausgehen, umso besser. Aber starten Sie erst einmal mit dem, was die Norm vorgibt. - Ihre Mitarbeiter ausbilden
Nicht nur, aber auch weil es die Norm verlangt, sollten Sie Ihre internen Auditoren systematisch ausbilden. Auch wenn es werblich klingt: Ziehen Sie auch das Seminar „Interner Auditor“ bei uns am Institut in Betracht. Dort lernen Sie genau das.




Guten Tag Herr Prof. Johner,
unsere benannte Stelle möchte von Jahr zu Jahr mehr Dokumente, schon vorab eines Audits, als digitale Version zur Einsicht erhalten. Früher wurde nur das Qualitätsmanagement-Handbuch gefordert. Mittlerweile sind Qualitätssicherungsrichtlinien, Standardverfahrensanweisungen und sogar Arbeitsprotokolle und Produktionsdokumentationen dazu gekommen.
Gibt es eine Liste welche Dokumente vorab von der benannten Stelle angefordert werden können?
Beste Grüße,
Dr. Andreas Breß
Sehr geehrter Herr Dr. Breß,
vielen Dank für Ihre wertvolle Anfrage.
Ich gehe davon aus, dass Ihre Benannte Stelle nicht nur das QMS nach ISO 13485 sondern auch Ihr(e) Produkt(e) nach der EU-Verordnung 2017/45 (MDR) prüft. Mittlerweile gehen die Notified Bodies dazu über, die Dokumente der technischen Dokumentation (MDR, Anhang II) vorab anzufordern. Sie sollten also die technische Dokumentation, soweit vorab gefordert, bei Ihrer Benannten Stelle einreichen.
Sehr geehrter Herr Prof. Johner,
vielen dank für die Informationen. Wir stellen IVDs her, fallen also erst in Zukunft vollständig unter die IVDR. Bis jetzt dürfen wir noch alle unsere Produkte ohne Beteiligung einer Benannten Stelle vertreiben. PMS ist natürlich jetzt schon gefragt aber diese Dokumente wollte die Benannte Stelle gar nicht im Vorweg einsehen. Natürlich wird sich dies mit der IVDR sich ändern. Ich war nur überrascht, dass die Benannte Stelle jetzt schon mit diesem Prozedere anfängt.