1. Definitionen
Zur medizinischen Software zählt alle Software, die für das Gesundheitswesen eingesetzt wird, insbesondere Software für Medizinprodukte bzw. Medizingeräte (Embedded Software) und Software, die selbst ein Medizinprodukt ist (Standalone-Software).
Die IEC/CD1 82304-1 (Health Software – Part 1: General requirements for product safety) unterscheidet folgende Begriffe:
- HEALTH SOFTWARE
Software intended to be used specifically for maintaining or improving health of individual persons, or the delivery of care
- MEDICAL SOFTWARE
Software intended to be used specifically for incorporation into a physical medical device or intended to be a SOFTWARE MEDICAL DEVICE
- SOFTWARE MEDICAL DEVICE
Software intended to be a medical device in its own right
- MEDICAL DEVICE SOFTWARE
Software intended to be used specifically for incorporation into a physical medical device
Damit wird klar, dass medizinische Software ein Medizinprodukt sein kann, aber nicht muss.
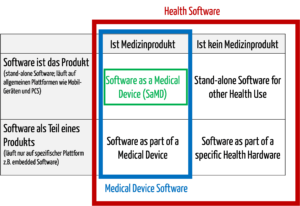
Abb. 1: Medizinische Software umfasst auch Medical Device Software und Software as a Medical Device (zum Vergrößern klicken).
2. Regulatorische Anforderungen
a) Medizinische Software – ein Medizinprodukt?
Es stellt sich oft die Frage, wann medizinische Software für die Medizintechnik der Definition des Begriffs Medizinprodukt entspricht. Eine weiterführende Diskussion dazu finden Sie im Artikel zur Klassifizierung von Software als Medizinprodukt sowie im Artikel zur Qualifizierung und Klassifizierung von IVD-Software.
b) Verordnungen, Gesetze, Normen
Software, die ein Medizinprodukt oder ein Teil dessen ist, muss die regulatorischen Anforderungen erfüllen:
- In Europa sind Medizinprodukteverordnungen (MDR, IVDR) relevant. Diese enthalten jedoch nur relativ allgemeine Vorschriften für Software, die dieser Fachartikel vorstellt.
- Die IEC 62304 definiert die Lebenszyklusprozesse für Software von Medizinprodukten.
- Die IEC 82304-1 ist bei jeder „Health Software“ anwendbar. Die IEC 82304-1 fordert auch Konformität mit den Anforderungen der IEC 62304.
- Es gibt zudem MDCG-Leitlinien z.B. die MDCG 2019-11 und die MDCG 2023-4.
- Die FDA stellt in ihren Guidance-Dokumenten spezifische Anforderungen, explizit auch an medizinische Software. Zudem beantwortete sie viele Fragen speziell zu Software as a Medical Device in diesem FAQ.
3. Unterstützung für Medizinproduktehersteller
Nutzen Sie die Unterstützung des Johner Instituts:
- Haben Sie Fragen zur Entwicklung und Zulassung von Medizinprodukte, die Software enthalten oder Software sind? Dann nutzen Sie das kostenfreie Micro-Consulting.
- Im Kompaktseminar Medizinische Software erwerben Sie die vorgeschriebenen Kompetenzen. Sie lernen die gesetzlichen Anforderungen an die Entwicklung von Software für die Medizintechnik kennen und erfüllen.
- Die Videotrainings des Auditgarant helfen Ihnen, Schritt für Schritt eine schlanke und IEC-62304-konforme „Software-Akte“ zu erstellen. Zusätzlich nimmt Ihnen ein vollständiger Satz an Templates viel Arbeit ab.
- Nutzen Sie auch die Unterstützung unserer Expertinnen und Experten. Sie helfen Ihnen, Ihre Software kurz, präzise und gesetzeskonform zu dokumentieren, und bereiten Sie auf Audits und „Tech File Reviews“ vor.
- Lassen Sie die IT-Sicherheit Ihrer Software durch Penetration Tests überprüfen.
Melden Sie sich gleich, damit wir die nächsten Schritte besprechen können. So stellen Sie sicher, dass die „Zulassung“ sicher gelingt und Ihre Software bzw. Ihre Produkte schnell in den Markt kommen.
Die Health Breach Notification Rule legt fest, wann Anbieter von Health Records welche Probleme mit der Datensicherheit an wen, in welcher Frist und in welcher Form melden müssen. Dieser Artikel verschafft Ihnen eine schnelle Übersicht über die Forderung der US-amerikanischen Federal Trace Commission (FTC).
Die Federal Trade Commission (FTC) ist eine US-amerikanische Behörde, deren Zielsetzung in der Wahrung des Wettbewerbsrechts und des Verbraucherschutzes liegt. Unter welchen Umständen Sie auch die Anforderungen der FTC beachten müssen und worin diese Anforderungen bestehen, lesen Sie in diesem Beitrag. Wie radikal die FTC auch bei Herstellern von Medical Apps vorgehen kann, zeigt der Fall Lumosity.
Details
„Findet ein Software-Audit statt?“ lautet eine Frage, die mich über unser Micro-Consulting erreicht. „Und kann ich durch eine geeignete Wahl der Software-Sicherheitsklasse so ein Software-Audit vermeiden?“ Erst ist mir weder klar, was genau mit „Software-Audit“ gemeint, noch was die genaue Befürchtung ist. Doch dann verstehe ich und finde die Frage sehr bedeutsam für alle Medizinprodukte-Hersteller.
Details
Software-Systemtest: Was versteht man genau darunter? Wann sind sie vorgeschrieben? Was sollten Software-Systemtests testen? Auf welche Fallen sollten Sie achten? Antworten gibt Ihnen dieser Beitrag.
Eine Schichtenarchitektur ist ein Architekturstil, der häufig bei Software-Systemen Anwendung findet. Vielen Herstellern sind die Nachteile eine mehrschichtigen Architektur und eines Denkens in Layern nicht bewusst.
Unter einem Hotfix verstehen die meisten Medizinprodukte-Hersteller die kurzfristige Behebung eines dringenden Software-Bugs. Bei diesen Hotfixes unterlaufen den Herstellern gravierende Fehler. Auch regulatorische. Lesen Sie hier, wie Sie die Software Ihrer Medizinprodukte durch einen Hotfix schnell und ohne Overhead aber dennoch gesetzeskonform updaten können.
Details
Die Risikoanalyse bei Software unterscheidet sich: Software selbst kann keine Schäden verursachen. Dies geschieht immer via Hardware oder Menschen. Doch das heißt nicht, dass es keiner Risikoanalyse bei Software bedarf. Im Gegenteil!
Der Begriff der Software-Einheit (englisch: Software Unit) entstammt der IEC 62304. Vielen Herstellern unterlaufen beim Spezifizieren und Testen dieser Software-Einheiten Fehler. Diese Artikel gibt Ihnen Tipps, diese zu vermeiden.
Details
Die IEC 60601-1 definiert ein PESS, ein programmierbares elektronisches Subsystem, als System, das auf einer oder mehreren zentralen Prozessoreinheiten beruht, einschließlich deren Software und Schnittstellen. Die Norm verrät nicht, was sie unter System versteht, es ist in diesem Kontext eine Komponente des Medizinprodukts. Dafür stellt die IEC 60601-1 konkrete Anforderungen an die PESS.
Details
Mit FHIR (gesprochen: Fire) hat HL7 einen modernen Interoperabilitätsstandard entwickelt, dem ich großes Zukunftspotenzial zutraue. Erfahren Sie mehr über Interoperabilität.
Details






