Medizinproduktehersteller müssen die Requirements (Anforderungen) an ihre Produkte ermitteln und nachweisen, dass diese erfüllt sind. Dabei kommt es häufig zu regulatorischen Problemen, auch weil es Missverständnisse mit den verschiedenen Typen an Requirements (Anforderungstypen) gibt.
Inhalt
Diese Seite verschafft einen schnellen Überblick über:
- Typen an Requirements/Anforderungen
- Regulatorische Anforderungen an diese Requirements
- Möglichkeiten der Unterstützung beim Erheben und Nachweisen
Zu allen Themen gibt es Verweise auf weiterführende Artikel.
1. Typen an Requirements / Anforderungen
Während der verschiedenen Entwicklungsphasen gilt es, die verschiedenen Typen an Anforderungen zu erheben und diese zu erfüllen (s. Abb. 1).
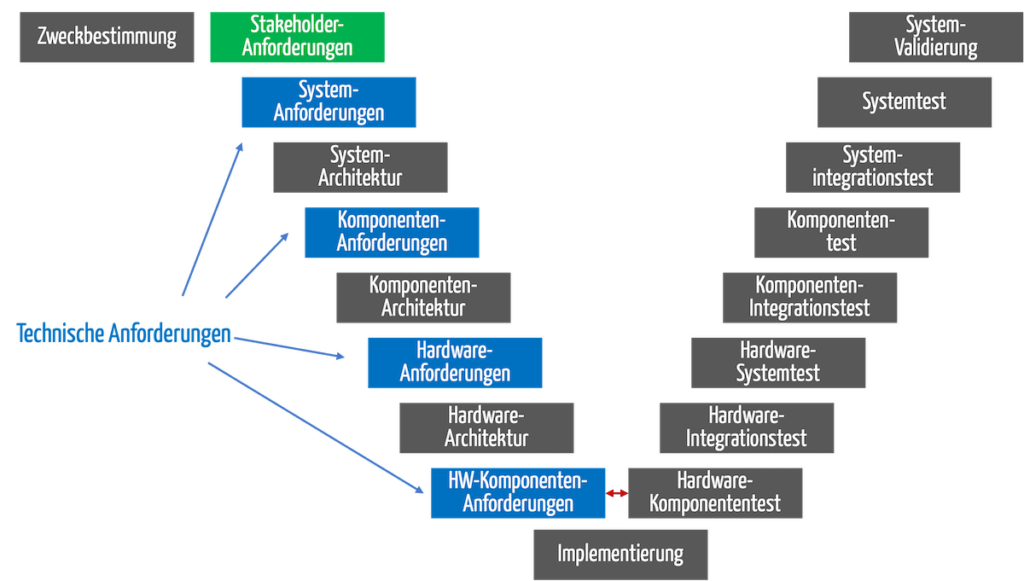
Abb. 1: Im V-Modell lassen sich die Phasen erkennen, in denen die Anforderungen erhoben werden. Stakeholder-Anforderungen (grün); technische Anforderungen (blau)
Die Stakeholder-Anforderungen und die technischen Anforderungen unterteilen sich in weitere Typen (s. Abb. 2).
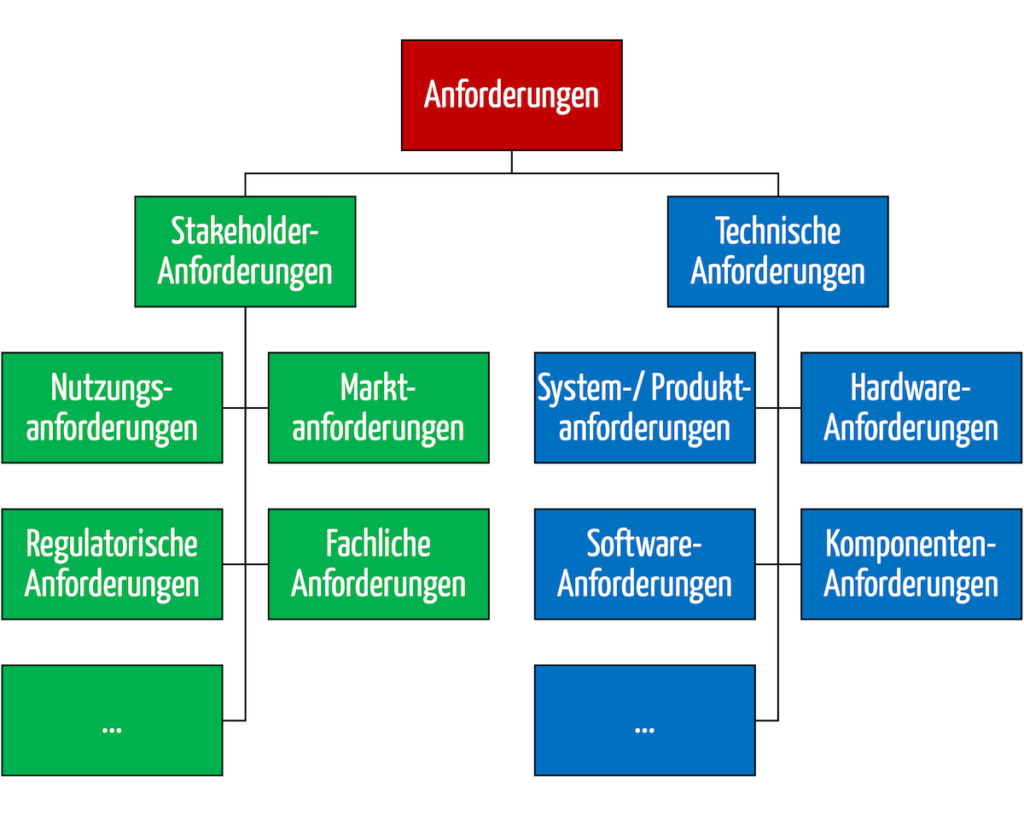
Abb. 2: Die Stakeholder-Anforderungen (grün) und die technischen Anforderungen (blau) haben jeweils Untertypen.
Weiterführende Informationen
Diese Artikel stellen Ihnen die verschiedenen Anforderungstypen mit den jeweiligen Methoden zum Erheben und Nachweisen sowie die regulatorischen Anforderungen daran im Detail vor:
2. Regulatorische Anforderungen
Es gibt regulatorische Anforderungen an die Requirements, konkret an das Erheben, Nachverfolgen und Nachweisen der Requirements.
a) Anforderungen an das Erheben von Requirements
Die regulatorischen Anforderungen an die Medizinprodukte verpflichten die Hersteller dazu, alle diese Typen an Anforderungen zu erheben und nachzuweisen.
Beispiele
- Die MDR verlangt, die relevanten grundlegenden Anforderungen zu bestimmen. Sie fordert Akzeptanzkriterien, beispielsweise bei klinischen Studien.
- Die IEC 62304 besteht auf Akzeptanzkriterien bei der Verifizierung der Software-Einheiten.
- Die IEC 62366-1 fordert Akzeptanzkriterien, konkret bei der Bewertung des User Interfaces.
- Die IEC 60601-1 spezifiziert zahlreiche Akzeptanzkriterien (z. B. maximale Ableitströme und Temperaturen), die sie auch als Prüfkriterien bezeichnet.
- Die ISO 13485 fordert, die Anforderungen der Kunden zu erheben, sowohl die explizit genannten als auch die nicht genannten. Sie verpflichtet die Hersteller dazu, alle regulatorischen Anforderungen zu identifizieren.
b) Anforderungen an das Tracing von Requirements
Aus den Gesetzen und Normen folgt auch, dass die Hersteller die Anforderungen nachvollziehen müssen. Hersteller sollten dabei zwei Arten der „Traceability“ unterscheiden:
- Horizontale Traceability
Die horizontale Traceability (gepunktete rote Linien in Abb. 3) soll sicherstellen, dass die Erfüllung aller Anforderungen auch tatsächlich bei der Verifizierung und Validierung überprüft wird.
- Vertikale Traceability
Die vertikale Traceability (gestrichelte rote Linien in Abb. 3) soll sicherstellen, dass die Anforderungen bei der weiteren Entwicklung tatsächlich berücksichtigt werden.
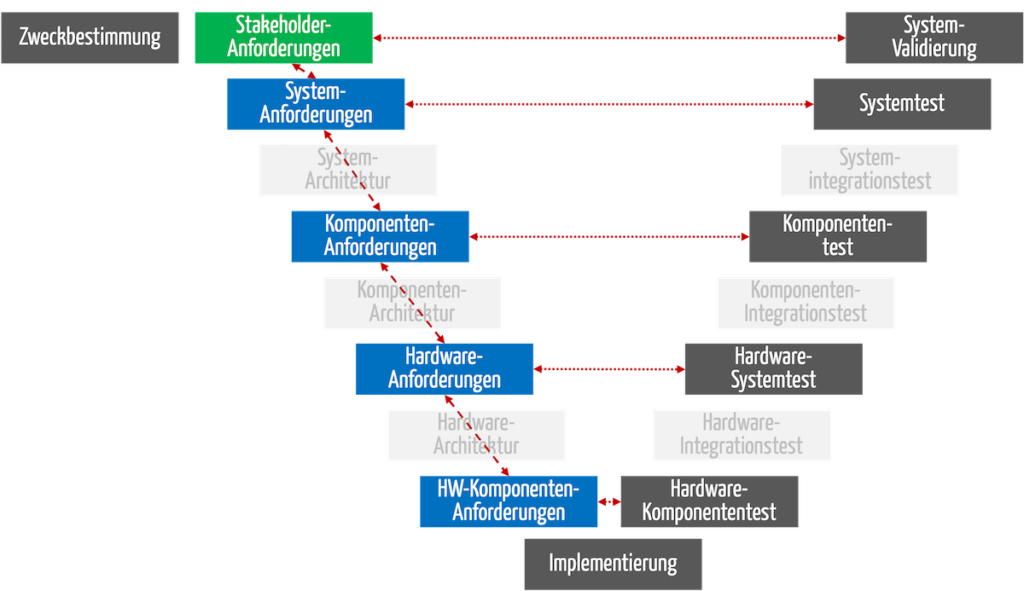
Abb. 3: Man unterscheidet horizontale Tracebaility (gepunktete Linien) und vertikale Traceability (gestrichelte Linien).
Die Traceability setzt voraus, dass die einzelnen Anforderungen eindeutig identifiziert sind, beispielsweise mit einer ID.
c) Anforderungen an den Nachweis von Requirements
Die Gesetze und Normen verpflichten die Hersteller nachzuweisen, dass die Produkte alle an sie gestellten Anforderungen erfüllen. Dabei setzen viele Hersteller Anforderungen mit Akzeptanzkriterien gleich. Auch wenn das in der Praxis oft funktioniert, sind die beiden Begriffe nicht synonym.
Akzeptanzkriterien beschreiben, woran man entscheidet, ob man eine Anforderung als erfüllt sieht.
Beispiel
Wenn eine Anforderung lautet, dass eine Software-Unit das Quadrat einer Zahl berechnen soll, dann lassen sich die Akzeptanzkriterien als die Testfälle formulieren, mit denen das geprüft wird. Aber die Testfälle sind nicht das Requirement.
Tipp
Das Johner Institut empfiehlt, dass die Systemanforderungen spezifizieren, wie sich ein System als Blackbox verhält.
Es gibt Akzeptanzkriterien, die nicht(!) diese Blackbox betreffen. Dazu zählt beispielsweise die Einhaltung von Kodierrichtlinien bei einer Software-Unit. Diese Einhaltung wäre keine Anforderung an die Software-Unit selbst, sondern an deren Entwicklung.
Dass die Akzeptanzkriterien erfüllt sind, ist notwendig, aber nicht hinreichend für den Nachweis, dass auch die Anforderungen erfüllt sind. Aber in der Praxis reicht der Nachweis erfüllter Akzeptanzkriterien meist als „objective evidence“ aus.
Unterstützung beim Erheben und Nachweisen der Requirements
Haben Sie noch Fragen zu den Requirements? Sie erhalten Antworten über unser kostenloses Micro-Consulting.
Im Seminar Usability, Requirements und IEC 62366-1 lernen Sie, die Anforderungen systematisch und normenkonform zu erheben.
Melden Sie sich, wenn Sie Unterstützung wünschen. Wir helfen Ihnen gerne dabei, schnell, einfach und gesetzeskonform alle relevanten Anforderungen zu erheben und nachzuweisen. Denn damit werden Ihre Produkte sicher und nachgefragt und kommen schnell in den Markt.