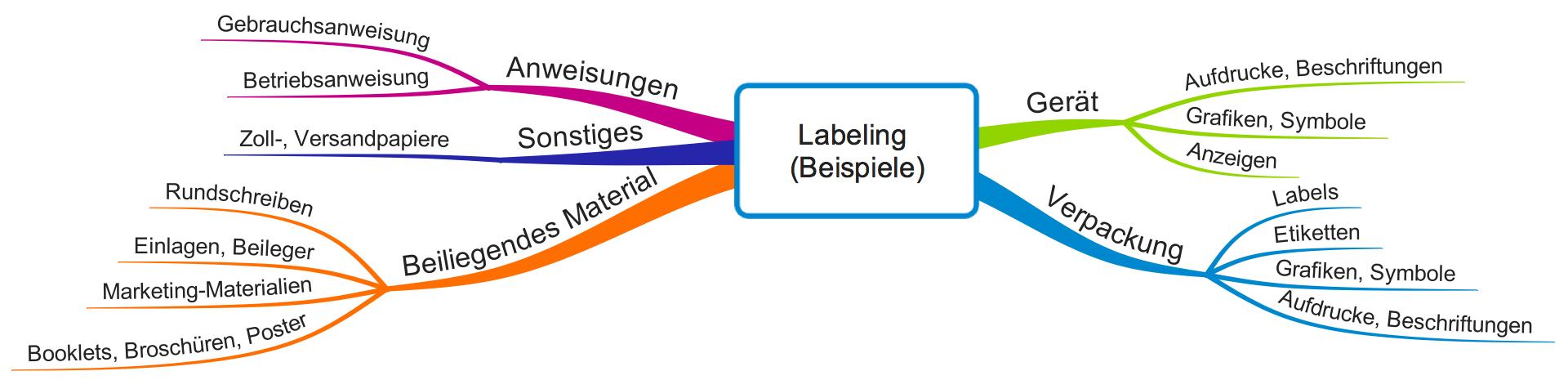
Usability Validierung: Konform mit IEC 62366-1 und FDA
Die Usability Validierung ist eine Prüfung mit objektiven Mitteln, ob spezifizierte Nutzer im spezifizierten Nutzungskontext die spezifizierten Nutzungsziele (Zweckbestimmung) effektiv und effizient erreichen können.